
「钽涂层专栏第四期」钽金属促成骨的生物学机制和信号通路(上)
发布时间:2022-06-01 11:28 浏览量:3703
引言
钽作为一种稀有难熔金属具有的绝佳理化性质和生物学特性。自从21世纪初多孔钽植入物被应用于骨和关节重建手术后,钽作为生物材料的优势表现明显,对比传统的钛和钛合金骨科植入物,大量体内、体外的实验室研究和临床实践均协同证明钽的成骨性能更好,成骨指标表达也更高。这些成骨指标包括碱性磷酸酶(ALP)、细胞矿化、I型胶原蛋白(COL I)、骨钙素(OCN)和骨桥蛋白(OPN)。
近年来,钽杰出的成骨性能背后蕴含的潜在机制被一一揭示,在这一期,我们将根据已发表的研究构建一张由钽激活的多种成骨信号通路组成的全景图。
一图流总结
骨骼再生是一个错综复杂的过程,涉及多个信号通路的激活或抑制,而不是简单的反应。
最近几年,研究者们揭示了钽与大量经典的成骨信号传导途径有关。如下表所总结的,包括Wnt/β-连环蛋白信号通路、 转化生长因子-β(TGF-β)和骨形态生成蛋白(BMPs)信号通路,丝裂原激活蛋白激酶(MAPKs)信号通路,以及整合素信号通路。
与钛组相比,钽组中成骨信号通路的关键分子表达量更高,这表明钽可以对与成骨有关的多种信号通路发挥积极作用。
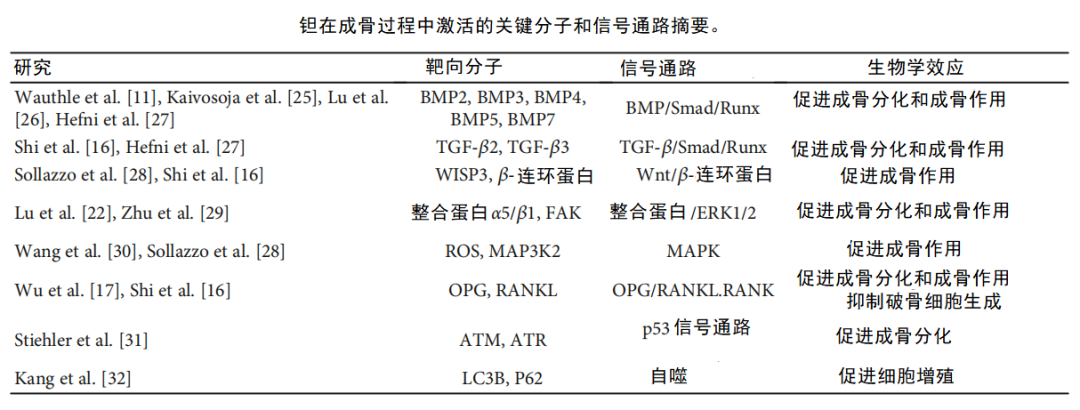
与钽有关的成骨信号传导途径详解
TGF-β超家族
信号通路解释
TGF-β超家族由骨形态发生蛋白(BMPs)亚组、TGF-βs、活化素、骨保护素(OPG)、核因子-κB受体活化因子配体(RANKL)和核因子-κB受体活化因子(RANK)组成。
TGF-β超家族成员可以与由两种受体(TGF-β1型和TGF-β2型)组成的跨膜异构受体复合物结合从而修饰细胞内的蛋白质和分子,经典Smad复合体途径和MAPK级联,以调节基因表达。
TGF-β超家族不仅在胚胎期的膜内和软骨内骨化中发挥重要作用,还通过调节成骨细胞和破骨细胞来协调成骨和溶骨。
TGF-β信号传导通路是一个包含众多成员的多功能细胞因子大家族,根据配体分子激活的不同的下游特异性通路可以分为TGF-β/Activin/Nodal和BMP/GDF/MIS两个亚家族通路。该信号通路的激活首先是TGF-βs配体分子与受体结合,从而使受体TβRs磷酸化,磷酸化的TβR-I直接作用于底物Smads蛋白,活化的Smads就将配体与受体作用的信号从细胞膜、胞浆传递到细胞核内,再与其他核内因子协同激活或者抑制靶基因的转录。
骨形态发生蛋白(BMPs)
骨形态发生蛋白(bone morphogenetic protein,BMP)又称骨形成蛋白,是一组具有类似结构的高度保守的功能蛋白,属于TGF-β家族。BMP能刺激DNA的合成和细胞的复制,从而促进间充质细胞定向分化为成骨细胞。它还是体内诱导骨和软骨形成的主要因子,并在肢体生长、软骨内骨化、骨折早期、软骨修复时表达,对骨骼的胚胎发育和再生修复起重要作用。
骨保护素(OPG)
OPG(骨保护素),又叫破骨细胞抑制因子(osteoclastogenesis inhibitory factor),是RANKL(破骨细胞分化因子)的诱导受体,通过与RANKL的结合减少破骨细胞的产生。OPG/RANKL/RANK系统是调控骨代谢的重要通路之一。成骨细胞表达的RANKL与破骨细胞表面RANK结合,可促进破骨细胞分化成熟。
核因子-κB受体活化因子配体(RANKL)
RANKL是破骨细胞分化因子,在成骨细胞中表达(osteoblast)可激活破骨细胞。RANKL过表达,可导致一系列骨疾病,如风湿性关节炎,银屑病性关节炎。
SMAD
Smads家族蛋白在将TGF-β信号从细胞表面受体传导至细胞核的过程中起到关键性作用,且不同的Smad介导不同的TGF-β家族成员的信号转导。TGF-β作为配体形成的受体复合物,激活Smads进入核内,共同激活或抑制它们调节的靶基因的转录。
血清碱性磷酸酶(ALP)
其中来自骨骼的ALP称为骨性碱性磷酸酶(bone alkaline phosphatase, B-ALP),主要存在于成骨细胞,占血清ALP的一半。当成骨细胞活性增强或骨形成增加时,血骨性碱性磷酸酶浓度升高,其血清半衰期为1-2天。
试验论据
Shi等研究者将人骨间质干细胞(hBMSCs)分别在钽和钛盘上进行共培养,观察到在钽盘上培养的hBMSCs有更高的ALP和钙结点表达。同时,在培养21天和28天后,Smad3的表达明显高于钽组,Smad3是参与激活TGF-β/Smads信号通路的一个关键蛋白。
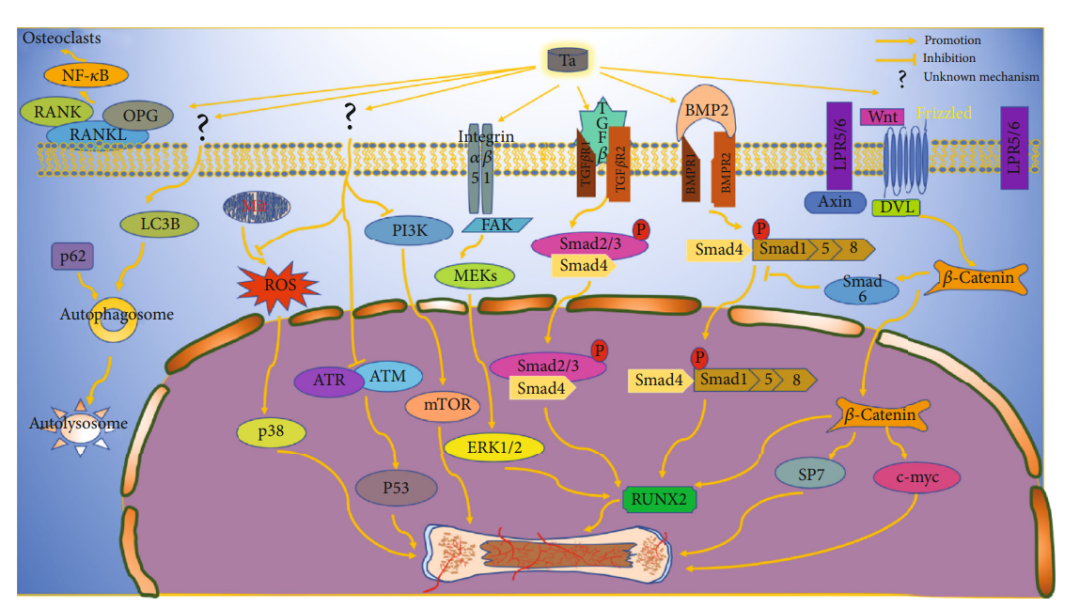
如图所示,钽触发的Smad2/3与Smad4相互作用并转入细胞核,从而激活成骨基因Runx2以促进成骨。为了进一步验证,用Smad3的特异性抑制剂(SIS3)进行预处理,以抑制TGF-β/Smad信号传导途径。有趣的是,随着SIS3的增加,ALP和钙结节的产生逐渐减少,这表明钽可能通过激活TGF-β/Smad信号传导途径来促进成骨。
同样,Hefni等将多孔钽小梁金属和钛圆柱体植入骨质疏松症患者的双侧下颌骨,发现与钛组相比,钽组的TGF-β3和TGF-β2在mRNA水平上有所上升。
这些结果协同表明,钽可以通过TGF-β信号通路促进成骨。
Runx2
Runx2作为转录因子Runt域家族成员的其中一个,其最初由人类基因组组织命名委员会(HUGO)采用了Runx这个术语来指代编码runt相关蛋白的基因。Runx2结合特定的DNA序列来调节众多基因的转录,从而控制间充质干细胞的成骨细胞发育、成熟为母细胞,在骨形成、软骨形成、骨代谢相关疾病方面起着重要的作用。
2021年由吴钰坤等发表于《中国组织工程研究》的52篇Runx2基因在骨愈合的作用机制荟萃研究显示:
Runx2在调控骨骼相关基因中发挥着重要作用,它不仅通过调节成骨细胞、软骨细胞、破骨细胞等骨细胞来调控骨吸收、骨形成与骨重建的过程,同时还可以与Wnt、骨形态发生蛋白/转化生长因子β信号传导通路,以及甲状旁腺激素、成纤维细胞生长因子分子之间相互作用来维持成骨细胞的形成和分化;
Runx2已经通过多项动物实验证实可对骨细胞分化增殖相关因素进行有效调控转录。
总 结
钽作为新世纪理想生物材料的卓越活性在骨科临床应用中得到了令人鼓舞的成功,本期介绍了钽成骨的根本机制之一“TGF-β信号传导途径”。
参考文献:
1. Qian, H., Lei, T., Ye, Z., Hu, Y., & Lei, P. (2020). From the Performance to the Essence: The Biological Mechanisms of How Tantalum Contributes to Osteogenesis. BioMed research international, 2020, 5162524. https://doi.org/10.1155/2020/5162524
2. 刘镕,赵琴平,董惠芬,蒋明森. TGF-β信号传导通路及其生物学功能[J].中国病原生物学杂志. 2014,9(01)
3. 吴钰坤, 韩 杰, 温帅波. 骨折愈合过程中Runx2基因的作用机制[J]. 中国组织工程研究, 2021, 25(14): 2274-2279.
版权所有 © 1998-2021 北京力达康科技有限公司 备案号:京ICP备14026466号  京公网安备 11011302003306号
京公网安备 11011302003306号