
TKA术后的假体-骨界面MRI分析
发布时间:2022-06-16 17:11 浏览量:2976

目的
本研究的目的是通过磁共振成像(MRI)来描述和表征TKA术后的股骨、胫骨和髌骨组件的假体-骨界接触面。
研究范围
从医疗记录筛选出55例采取TKA且术后接受MRI的患者进行回顾性分析,MRI图像已修改以减少伪影。其中27例TKA采用锆成分,28例采用传统钴/铬/钼合金成分(CoCrMo)。
核磁图像由两位盲法独立研究者评估,并采用Cohen’s Kappa来确定观察者间的可靠性。
由锆制成的胫骨、髌骨和股骨假体的界面具有良好的可视性、可靠性和观察者间的一致性。传统的CoCrMo组件造成了明显的伪影,干扰了股骨组件界面的评估。
结论
采用特殊方案进行的MRI对TKA术后胫骨和髌骨假体-骨界面分析具有良好的重现性。
由锆制成的股骨假体与骨界面可以识别。传统的CoCrMo股骨组件造成了相当大的伪影,并干扰了股骨界面的评估。为降低金属敏感性伪影而定制的MRI可以作为评估假体与骨界面的有效工具,并可能有助于对诊断假体的松动。
01简介
在全膝关节置换术(TKA)中,稳定的固定和合理的骨水泥渗透被认为是植入物寿命的一个重要特征。TKA作为针对膝关节炎治疗的成功方法,假体在术后10年的存活率高于90%[2-4]。尽管总体失败率较低,但无菌性松动和磨损引发的初次TKA手术翻修仍然呈上升趋势[5]。
传统的X光片和计算机断层扫描(CT)对界面的评估是有限的,而且CT还会使病人受到大量的辐射。MRI由于金属植入物会产生强烈伪影,对全膝置换术后评估疗效也一直较低[6],研究主要集中在对韧带、肌腱和颗粒疾病的评估[6,9]。
但随着材料和技术手段的提升,通过合理的修正,MRI已被用于评估全髋关节置换术后髋关节病变[7]、全膝关节置换术后疼痛[6]和关节运动学[8]。
锆质股骨组件具有安全、有效、减少PE磨损的特点[10]。锆允许高质量的核磁共振成像,只要对脉冲序列和成像参数做一些改变就能最大限度地减少通常由金属植入物引起的图像伪影,实现高质量的MRI。这要归功于其较低的磁矩[10,11],在临床上可用于评估假体周围结构[11]。
本研究的目的是利用MRI来描述TKA后股骨、胫骨和髌骨组件的植入物-骨界面的特征。比较传统股骨钴/铬/钼合金(CoCrMo)和锆合金组件使用MRI成像后评估植入物-骨界面的可靠性和可重复性。
02患者和方法
从医疗记录中回顾性地找出在TKA后接受膝关节MRI检查的患者纳入研究,包括36名女性和19名男性共55名患者,平均年龄为59.1±11.1岁(23名左膝,32名右膝)。所有患者都因退行性关节疾病接受了TKA手术。
MRI检查是在指数手术后平均间隔23.7±28.7个月进行的。27名患者采用了后稳定(PS)Genesis II,股骨锆组件(Oxinium™,Smith and Nephew,Memphis,TN,USA)。28名患者使用了传统的CoCrMo合金股骨组件。相应的胫骨组件是模块化的,在钛/铝/钒合金底板(TiAlV)上有一个聚乙烯(PE)垫片。
(核磁共振成像流程略,可关注北京力达康公众号“bjldk98”,后台留言“MRI”获得)
股骨、胫骨和髌骨组件的组件-骨界面通过评分(表1)进行评估。

"0":由于金属伪影,界面不可见;
"1":无骨吸收,组件与下层骨之间无间隙;
"2":间隙小于2mm;
"3":间隙大于2mm或骨溶解(图1)。
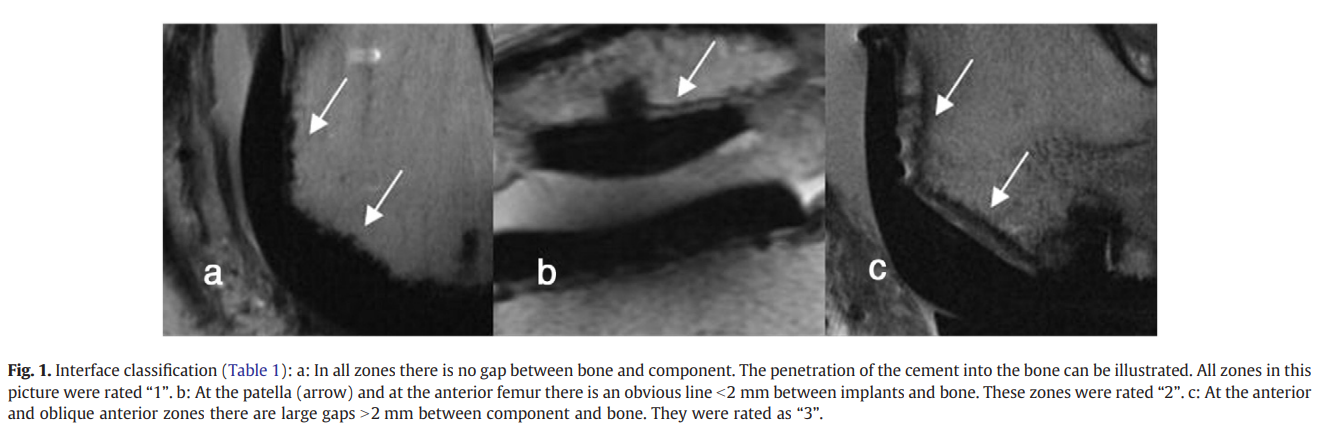 根据在TKA中进行的标准化骨切割,将界面分成不同的区域。在股骨侧,它被区分为前部、前部斜面、远端。后部斜面和后部表面,记录每个股骨上的位置(外侧和内侧)。
根据在TKA中进行的标准化骨切割,将界面分成不同的区域。在股骨侧,它被区分为前部、前部斜面、远端。后部斜面和后部表面,记录每个股骨上的位置(外侧和内侧)。
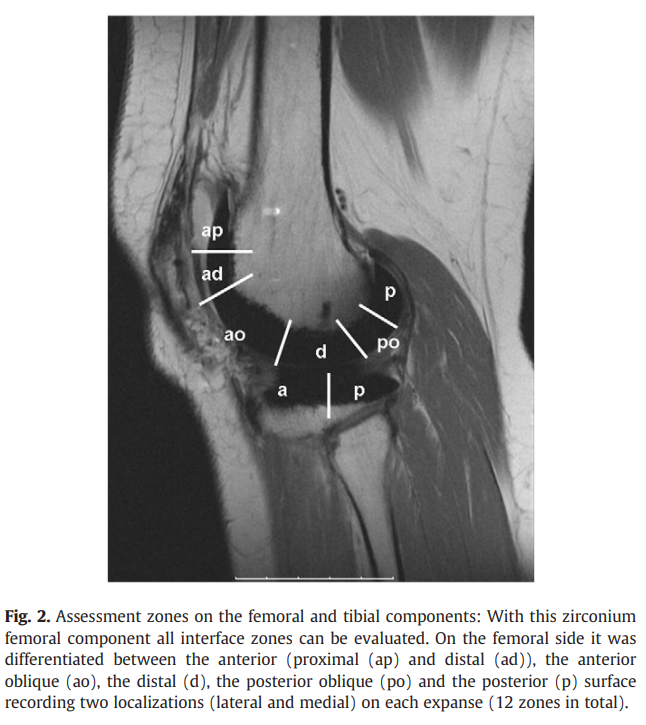
因此,对每个股骨组件进行了12个区域的评估(图2)。对于胫骨部分,前部和后部平台以及胫骨柄分别在内侧和外侧进行评分。分别对内侧和外侧进行评分,相当于六个区域。髌骨被细分为四个象限并进行评分。总共有22个界面。
连续变量以平均值和SD表示。分类数据用绝对值表示。对于数据的分析,P小于0.05被认为是有统计学意义的。在验证了平等分布后,用t检验对数值进行分析。核磁共振图像由两位独立的审查员(L.C.和T.H.)进行评估,他们没有获得临床信息且没有参与过手术。他们的结果值被用来作为计算Cohen's Kappa来确定观察者间的可靠性。
依照使用手册,Kappas超过0.75为优秀,0.40至0.75为一般,而低于0.40为差。统计分析使用Microsoft Excel (Microsoft Corporation, Seattle, USA) 和IBM SPSS统计18(PASW 18,SPSS公司,芝加哥,IL,美国)。
03结果
分析了两种不同的股骨头组件(CoCrMo和锆)。
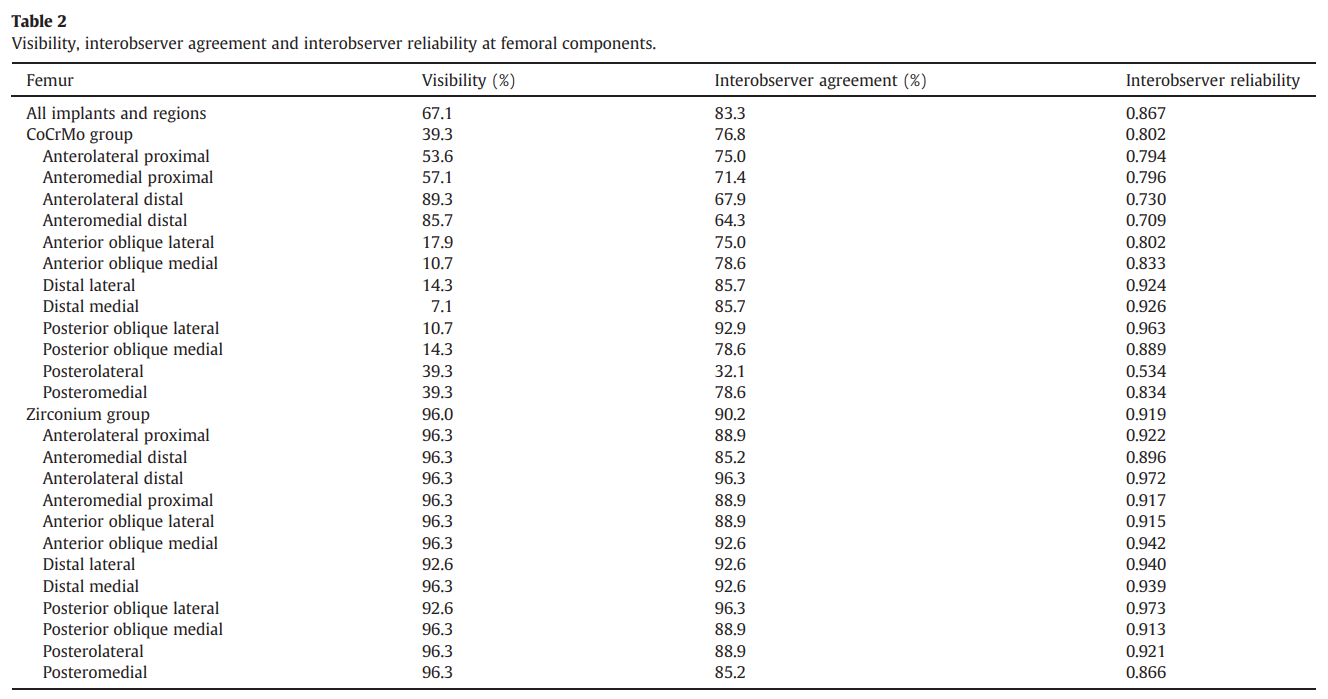
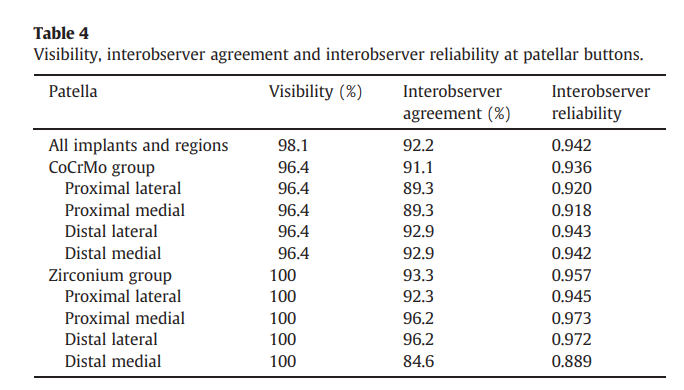
在CoCrMo组,股骨组件的Cohen's Kappa平均为0.802(表2)。胫骨组件为0.954(表3),髌骨组件为0.936(表4)。表明审查员之间的可靠性很高,特别是对于胫骨和髌骨。
在CoCrMo组中所有组件审查员之间的可靠性为0.80,可见度为48.9%;观察者之间的可靠性为0.936,能见度为48.9%,审查员之间的一致性为84.6%。特别是对于股骨组件,由于金属伪影的存在,可见的界面区比例很低(19.6%)(图3)。
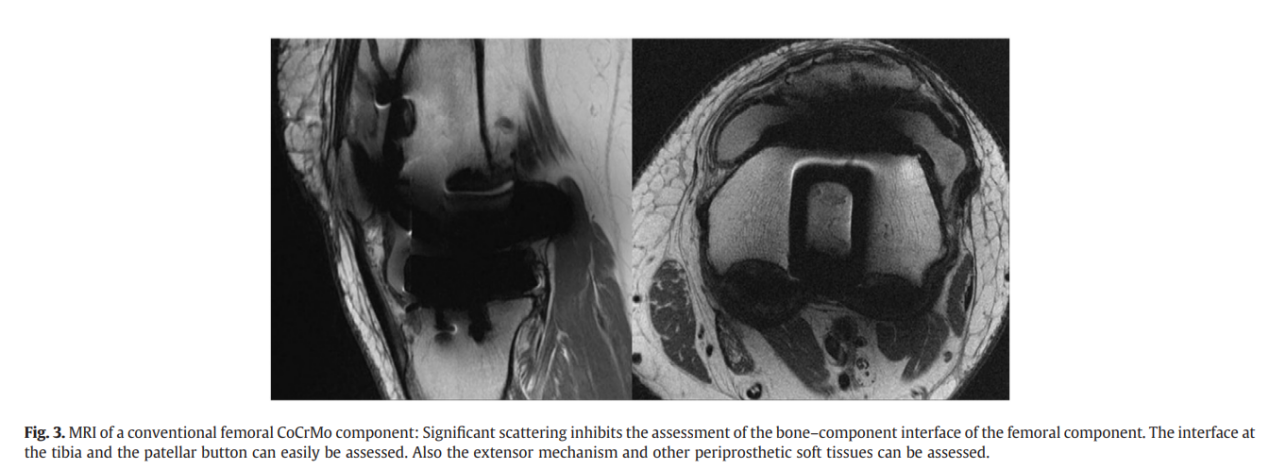
在前缘,74.6%的膝关节能够被评估。伪影干扰了评估,特别是在股骨远端边缘(只有13.4%的膝关节在这个区域可以解读)、后斜面(16.1%)、前斜面(19.6%)和后缘(36.6%)。尽管股骨组件造成了伪影,但在大多数情况下,胫骨组件(95.8%)和髌骨按钮(91.1%)都容易评估。由于伪影的存在,两位审查员对CoCrMo股骨组件的一致性最低(76.8%)。胫骨(95.8%)和髌骨(91.1%)的评估没有受到CoCrMo股骨组件造成的伪影的影响,从而有较高的一致率。所有的数值都显示在表2-4中。
在锆组中,Cohen's Kappa平均为0.919(表2),胫骨部件为0.956(表3),髌骨为0.957(表4),表明所有部件的审查员间可靠性很高。在这一组中,伪影十分罕见。对于所有部件,审查员之间的可靠性为0.83,可见度为97.8%,观察者之间的一致性为91.1%。伪影只干扰了股骨组件的少数界面区(96.0%)。这主要是由于在一个病例中,股骨组件是用传统合金制成的柄插入的。
胫骨(100%)和髌骨部件(100%)没有受到植入部件产生的少量伪影的影响。对于股骨(90.2%)、胫骨(93.3%)和髌骨组件(90.8%),调查者之间的一致性很高(表2-4)。
表2-4显示了观察者之间的可靠性,所有区域和植入物都显示出优秀的数值。

讨论和总结
目前的数据显示,应用新的主观MRI评分,在TKA后对骨-组件界面的分析具有良好的可重复性。
锆有利于股骨组件的分析,股骨的所有界面区域都可以解释。铬钼合金部件产生的伪影明显更多,因此无法对股骨部件上的大多数接触面进行评分。
在确定分数时,两位审查员在胫骨和髌骨假体之间的一致性较低。对胫骨和髌骨的评估几乎没有受到CoCrMo股骨组件的伪影影响。它们的接触面大部分都得到了充分的成像,审查员们对这两种组件的一致性远远超过90%,具有很高的可靠性。
高磁场时,金属植入物往往会被磁化,这与磁化程度低的身体组织形成鲜明对比。容易被磁化的金属植入物和磁化程度低的软组织包膜在解剖学上的紧密并列,会干扰MRI的评估,导致金属产生的伪影[12]。这些伪影的具体例子包括信号空洞、图像失真、对比度损失和信号不均匀性[9,12]。金属伪影的大小主要取决于设备的方向、磁场的强度和金属的类型[8,12]。某些材料是铁磁性的,这意味着它们即使在去除外部磁场后仍然被磁化,因此能够干扰核磁共振成像。除了钴、铬和钼之外,镍也是铁磁性的,大大增加了金属伪影和磁场不均匀性[11]。
膝关节置换术后的MRI成像需要一定的学习曲线,才能获得最佳的成像。成像结果也受到遵循的MRI方案影响。核磁共振成像中弥漫性和周向性的骨吸收通常是组件松动的提示。
过去,Potter等人报道了一些病例中MRI被证明有助于评估疼痛或无功能的TKA(关节纤维化、滑膜炎、松动、慢性感染、骨质疏松症、关节炎)[9]。有两份报告(分别评估了11名和2名患者[13,14])对TKA术后放射性疑似假体周围骨质疏松症进行了成功评估。
最近,核磁共振被提倡用于评估TKA后体内的运动学[8,15]。总之,MRI是评估疼痛的一个强有力的工具。但目前还没有建立标准的诊断标准,未来的工作必须关注TKA周围MRI的适应症和诊断标准以提供一个可重复的组件-骨界面的评分。
此外,这项技术是研究植入物设计和固定对骨水泥界面影响的一个有用工具。目前的研究表明锆合金股骨组件可以改善MRI中界面的可见性。为减少金属伪影而定制的MRI可能有助于诊断TKA后的松动。

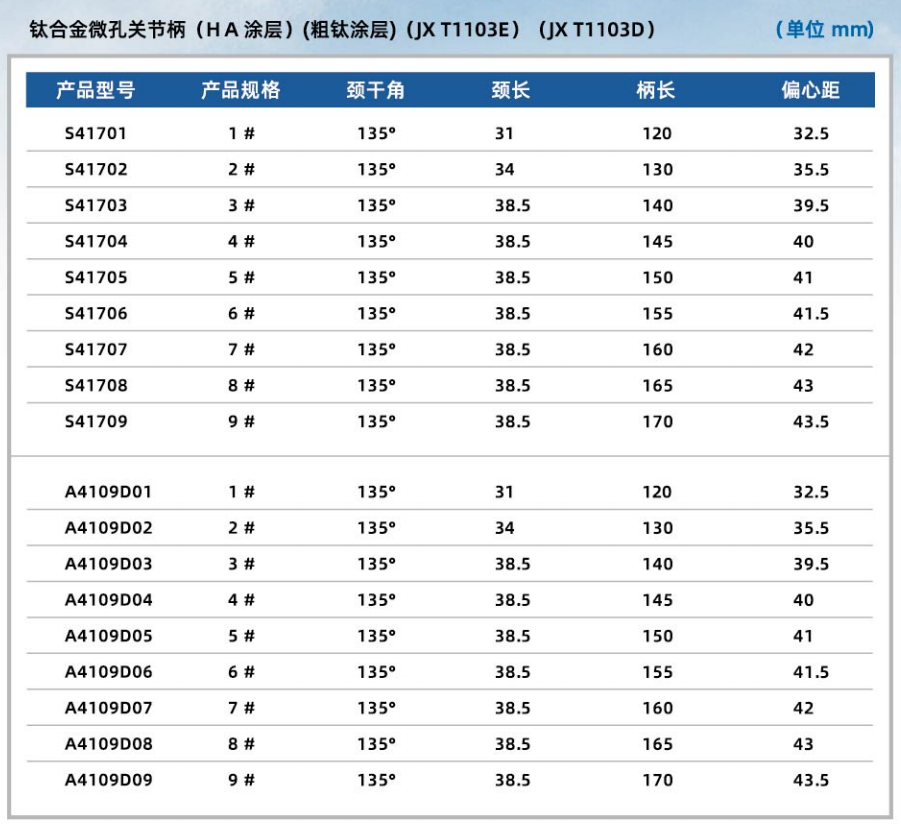
钛合金微孔关节柄(HA涂层)(粗喷钛涂层)
12/14标准锥度,缩窄的颈部设计,增加关节活动范围。
近端梯形横断面提供轴向和旋转稳定性。
提供HA涂层及双喷涂层三种股骨柄。
外侧削肩设计,易于植入,降低术中大粗隆骨折风险。
近端阶梯状设计,在假体植入时剪切力转化为压应力,既增强了假体植入时初始稳定性,又增加了与松质骨的接触面积,提升骨长入效果。
纵向沟槽和涂层提供抗旋转稳定性,避免远端大腿疼痛。

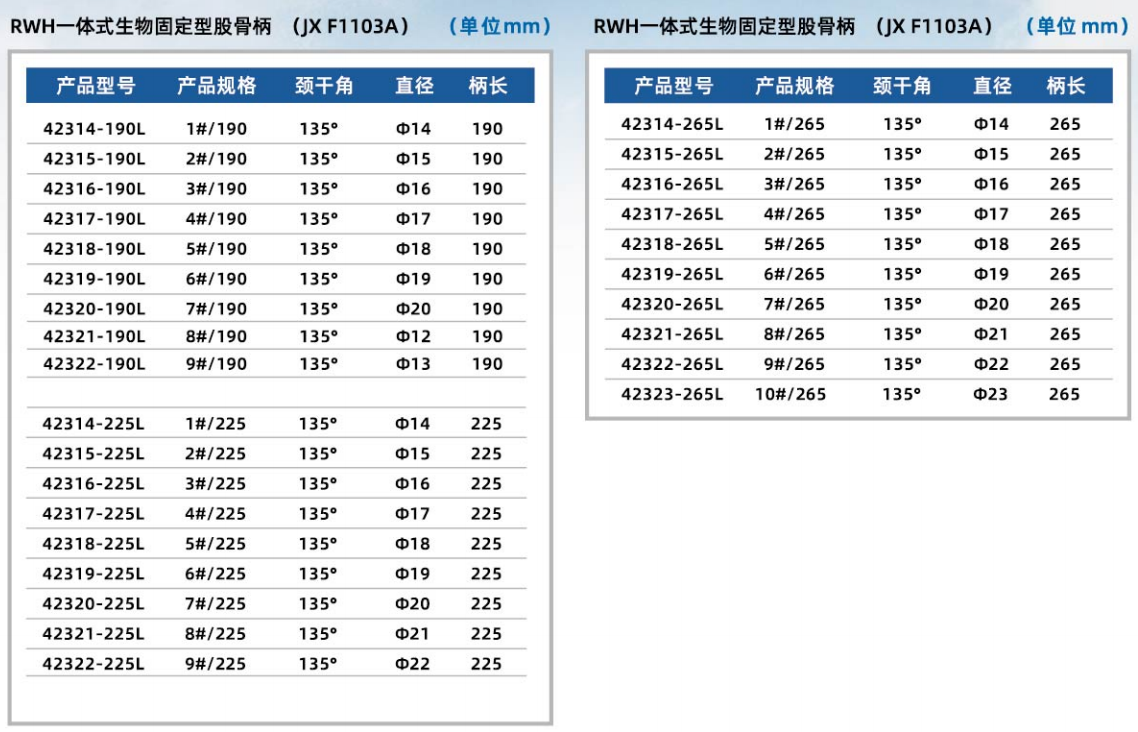
RWH一体式生物固定型股骨柄
同类柄型产品拥有超过20年优异临床结果,瑞典国家髋关节统计中心推荐翻修柄。
锻造钛合金材质,一体式锥形柄型。
柄体2°锥度,有效防止下沉,可任意调节前倾角。
8条纵形脊,提高良好的初始稳定和防旋转效果。
多种长度190-265mm。
文献参考:
[1]Heyse, T. J., Chong, l., Davis, J., Boettner, F., Haas, S. B., & Potter, H. G. (2012). MRI analysis of the component-bone interface after TKA. The Knee, 19(4), 290–294.
[2] Rodriguez JA, Bhende H, Ranawat CS. Total condylar knee replacement: a 20-year followup study. Clin Orthop Relat Res2001;388:10–7.
[3] Callaghan JJ, Squire MW, Goetz DD, Sullivan PM, Johnston RC. Cemented rotating platform total knee replacement. A nine to twelve-year follow-up study. J Bone Joint Surg Am 2000;82(5):705–11.
[4] Pradhan NR, Gambhir A, Porter ML. Survivorship analysis of 3234 primary knee arthroplasties implanted over a 26-year period: a study of eight different implant designs. Knee 2006;13(1):7–11.
[5] Sharkey PF, Hozack WJ, Rothman RH, Shastri S, Jacoby SM. Insall award paper. Why are total knee arthroplasties failing today? Clin Orthop Relat Res 2002(404): 7–13.
[6] Sofka CM, Potter HG, Figgie M, Laskin R. Magnetic resonance imaging of total knee arthroplasty. Clin Orthop Relat Res 2003;406:129–35.
[7] White LM, Kim JK, Mehta M, Merchant N, Schweitzer ME, Morrison WB, et al. Complications of total hip arthroplasty: MR imaging-initial experience. Radiology 2000;215(1):254–62.
[8] Lee KY, Slavinsky JP, Ries MD, Blumenkrantz G, Majumdar S. Magnetic resonance imaging of in vivo kinematics after total knee arthroplasty. J Magn Reson Imaging 2005;21(2):172–8.
[9] Potter HG, Foo LF. Magnetic resonance imaging of joint arthroplasty. Orthop Clin North Am 2006;37(3):361–73 vi-vii.
[10] Heyse TJ, Davis J, Haas SB, Chen DX, Wright TM, Laskin RS. Retrieval analysis of femoral zirconium components in total knee arthroplasty preliminary results. J Arthroplasty 2011 Apr;26(3):445–50. Epub 2010 Feb 9.
[11] Raphael B, Haims AH, Wu JS, Katz LD, White LM, Lynch K. MRI comparison of periprosthetic structures around zirconium knee prostheses and cobalt chrome prostheses. AJR Am J Roentgenol 2006;186(6):1771–7.
[12] Harris CA, White LM. Metal artifact reduction in musculoskeletal magnetic resonance imaging. Orthop Clin North Am 2006;37(3):349–59 vi.
[13] Mosher TJ, Davis III CM. Magnetic resonance imaging to evaluate osteolysis around total knee arthroplasty. J Arthroplasty 2006;21(3):460-3.
[14] Vessely MB, Frick MA, Oakes D, Wenger DE, Berry DJ. Magnetic resonance imaging with metal suppression for evaluation of periprosthetic osteolysis after total knee arthroplasty. J Arthroplasty 2006;21(6):826–31.
[15] Carpenter RD, Brilhault J, Majumdar S, Ries MD. Magnetic resonance imaging of in vivo patellofemoral kinematics after total knee arthroplasty. Knee 2009;16(5): 332–6.
版权所有 © 1998-2021 北京力达康科技有限公司 备案号:京ICP备14026466号  京公网安备 11011302003306号
京公网安备 11011302003306号